“Affinché non si ripresentino possibili epidemie di ritorno nei prossimi 18 mesi e prima che sia disponibile un possibile vaccino, è doveroso da parte della comunità scientifica individuare strategie terapeutiche efficaci e tempestive.” Questo l’obiettivo su cui si impegna il progetto CoronAid il progetto coordinato dal Dr Stefano Casola dell’IFOM di Milano, vincitore di un finanziamento FC, FUV e Regione Lombardia in partnership con l’Università degli Studi di Brescia, ASST Spedali Civili di Brescia, Università degli Studi di Milano, ASST Santi Paolo e Carlo di Milano, e l’IBM di Zurigo.
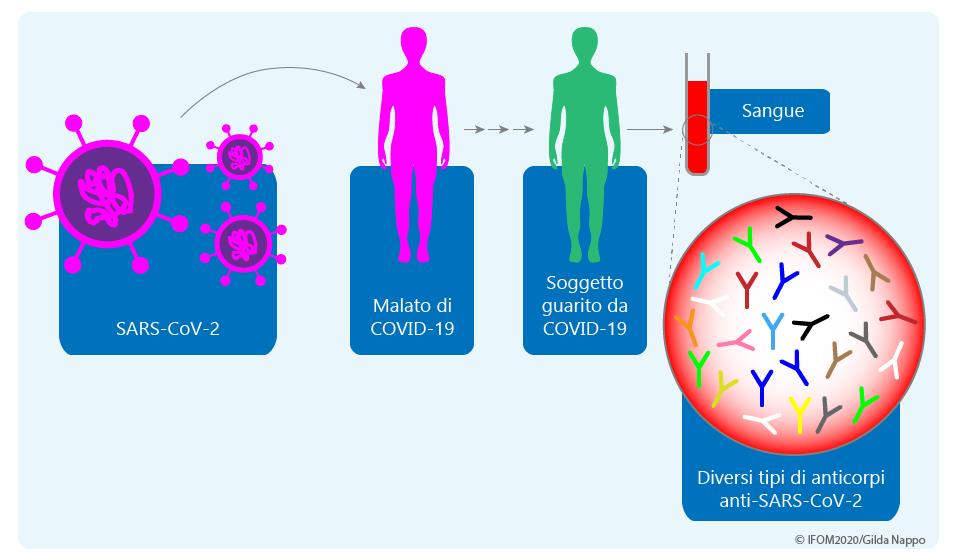
“Barriere essenziali all’ingresso e alla disseminazione nell’organismo di SARS-CoV2 sono gli anticorpi, proteine prodotte e rilasciate da linfociti B in seguito al contatto diretto con il virus. – illustra Casola, esperto di linfociti B di levatura internazionale – Ma ad oggi, la conoscenza delle dinamiche della produzione anticorpale di pazienti COVID-19 in risposta al contatto con SARS-CoV2 rimane limitata a causa di una carenza di test sierologici che permettano una misurazione sensibile, specifica e soprattutto quantitativa di anticorpi prodotti contro il virus.” “Inoltre – precisano i Professori Raffaele Badolato e Giulia Marchetti rispettivamente dell’ Università di Brescia (ASST Spedali Civili di Brescia) e dell’Università di Milano (ASST Santi Paolo e Carlo) – ancora non disponiamo di metodi diagnostici preposti al dosaggio delle distinte classi e sottoclassi di anticorpi prodotti in risposta al contatto con il virus.” Questa conoscenza risulta fondamentale in quanto diverse classi (es IGM IGG, IGA) e sottoclassi (IGG1, IGG2, IGG3 e IGG4) di anticorpi svolgono funzioni distinte nel corso dell’infezione, con alcune (sotto)classi che partecipano al processo infiammatorio aggravandolo, mentre altre agiscono neutralizzando l’entrata del virus nelle cellule bersaglio. “Pertanto – proseguono Badolato e Marchetti – un test diagnostico per la misurazione quantitativa e selettiva della frazione di anticorpi neutralizzanti prodotti contro il virus SARS-CoV2 rappresenta una priorità assoluta.”
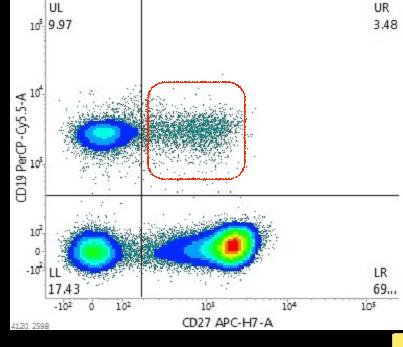
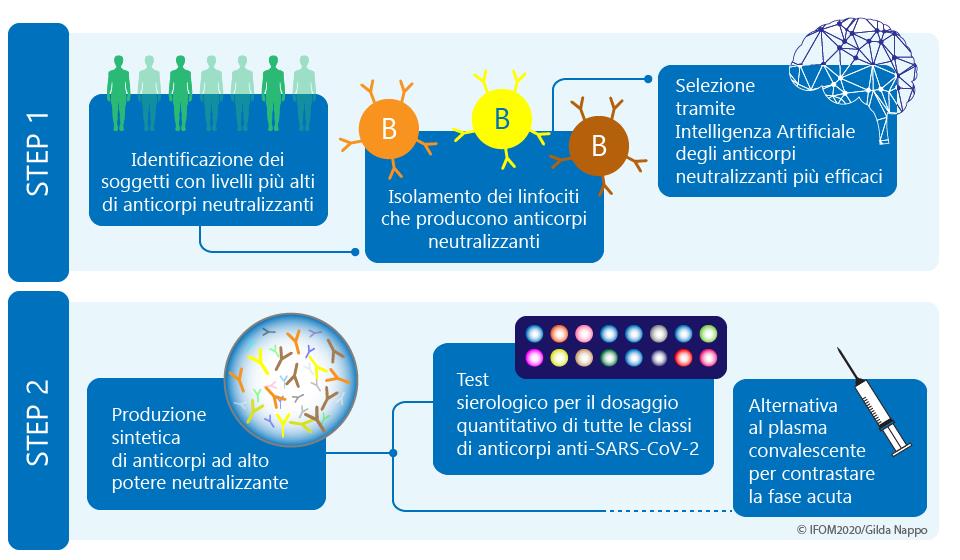
Un progetto ambizioso, percorribile solo grazie alla stretta sinergia da cui è nato il progetto, che integra le conoscenze complementari di un pool di ricercatori multicentrico con esperienza avanzata nei campi di immunologia cellulare, molecolare, di genetica degli anticorpi e di modelli matematici basati su Intelligenza artificiale e struttura degli anticorpi. Come verrà condotto il progetto CoronAId? Applicando metodiche avanzate di immunogenetica allo studio di linfociti B isolati dal sangue di un gruppo selezionato di individui che hanno contratto l’infezione del virus SARS-CoV2 sia in età adulta che pediatrica, e curati presso gli istituti clinici ASST Spedali Civili di Brescia e l’ASST Santi Paolo Carlo di Milano, i ricercatori di IFOM, in collaborazione con l’Istituto di Medicina Molecolare “A. Nocivelli” ricostruiranno il patrimonio complessivo di anticorpi prodotti da linfociti B reclutati nella risposta immune contro il virus. “Si tratta – precisa Casola – di applicare ai linfociti B reclutati nella battaglia contro il virus le stesse procedure sperimentali che utilizziamo per diagnosticare la natura maligna di linfomi e leucemie che colpiscono occasionalmente le stesse cellule.” “In stretta sinergia con la Dr.ssa Rodriguez Martinez del centro IBM di Zurigo, – continua il Prof Camilloni dell’Università di Milano – utilizzeremo algoritmi e modelli matematici basati su Intelligenza artificiale e analisi di banche dati di interazioni anticorpi-antigene, per estrapolare dai dati genetici sulle immunoglobuline prodotti in IFOM, informazioni rilevanti per selezionare il gruppo di anticorpi anti-SARS-CoV2 con spiccata proprietà di neutralizzazione del virus”. Questi anticorpi, una volta sintetizzati in laboratorio, serviranno come reagenti per lo sviluppo di un test sierologico (il primo del suo genere) che garantisca un dosaggio accurato delle concentrazioni di tutte le classi e sottoclassi di immunoglobuline prodotte contro la proteina Spike del virus SARS-CoV2. Gli anticorpi sintetici che mostreranno il più alto potere neutralizzante in modelli pre-clinici di infezione da SARS-CoV2 promettono di diventare una valida alternativa al plasma convalescente per contrastare la fase acuta di infezioni da SARS-CoV2.
“Le prospettive che apre CoronAId – spiega Casola – sono di mettere il primo test sierologico quantitativo per il dosaggio di tutte le classi di anticorpi anti-SARS-CoV2, a disposizione di ospedali e istituti di ricerca per sostenere studi a carattere scientifico e clinico di natura epidemiologica e di monitoraggio longitudinale dell’immunità acquisita contro SARS-CoV2.” In una fase in cui un vaccino non è ancora disponibile, gli anticorpi neutralizzanti sintetizzati in forma ricombinante diretti contro SARS-CoV2 hanno il potenziale per diventare un’arma decisiva nelle mani della comunità dei medici per prevenire ed eventualmente bloccare le gravi manifestazioni cliniche della malattia COVID-19 in pazienti contagiati dal virus.
“Ringrazio – conclude Casola – i nostri partner progettuali senza cui non sarebbe stato possibile concepire un progetto di così ampio respiro, che collega con un filo diretto il bancone di laboratorio, le più avanzate tecnologie immunogenetiche, l’intelligenza artificiale e la conoscenza clinica. E ovviamente grazie a Regione Lombardia, Fondazione Cariplo e Fondazione Umberto Veronesi per aver creduto nel nostro progetto e nella sua carica innovativa”.
La squadra di Coronaid

Dr. Stefano Casola (Istituto FIRC di Oncologia Molecolare, IFOM, Milano): Promotore dello studio. Esperienza in immunologia cellulare e molecolare con focus su linfociti B e sulla genetica degli anticorpi. L’unità sarà responsabile della generazione di librerie di geni anticorpali da linfociti B isolati da pazienti COVID-19 convalescenti. L’unità si occuperà anche della sintesi in forma ricombinante di anticorpi umani anti-SARS-CoV2 a potere neutralizzante, della loro validazione pre-clinica e dello sviluppo di un test sierologico ELISA per la quantifica dei livelli circolanti di tutte le classi e sottoclassi di anticorpi anti-SARS-CoV2.

Prof Raffaele Badolato (Spedali Civili di Brescia e Università di Brescia): esperienza in studi delle basi cellulari dei difetti immunitari di pazienti con immunodeficienze congenite. L’unità sarà responsabile della raccolta del materiale biologico da pazienti COVID-19 pediatrici e collaborerà con l’Unità del Dr Casola nell’isolamento di linfociti B reattivi contro il virus SARS-CoV2.

Prof. Giulia Marchetti (Università degli Studi di Milano, ASST Santi Paolo e Carlo, Milano): esperienza di immunologia cellulare nel contesto di diverse malattie infettive. L’ unità sarà responsabile della raccolta del materiale biologico da pazienti COVID-19 adulti e collaborerà con l’Unità del Dr Casola nell’isolamento di linfociti B reattivi contro il virus SARS-CoV2.

Dr.ssa Maria Rodriguez Martinez (IBM, Zurigo): esperienza nello sviluppo di modelli matematici basati su Intelligenza Artificiale. La sua unità contribuirà a selezionare dalla libreria di geni IGV espressi da linfociti B memoria di pazienti Covid-19, quelli a più alta affinità e potere neutralizzante contro proteina Spike di SARS-CoV2.

Prof. Carlo Camilloni (Università degli Studi di Milano): esperienza in analisi computazionali di biologia strutturale. La sua unità integrerà informazioni ottenute da approcci basati sull’ uso di intelligenza artificiale e biologia strutturale per contribuire a selezionare anticorpi neutralizzanti diretti contro la proteina Spike di SARS-CoV2.
